http://concurso.cnice.mec.es/cnice2005/93_iniciacion_interactiva_materia/curso/materiales/enlaces/enlaces1.htm
Enlaces Químicos, clases de enlaces y propiedades periódicas
https://www.youtube.com/watch?v=JUxg4XKRbW0
https://www.youtube.com/watch?v=6sycXHKHY0Y
https://www.youtube.com/watch?v=iTaFPJGfFH0&list=PLC866F66CA4E9DD1E
Observa el movimiento del electrón. El sodio se transforma en catión y el cloro en anión
Esta regla inidca que cuando se van a enlazar dos átomos iguales, los electrones de valencia de éstos se organizan de tal manera que, al formar el enlace por compartición de pares de electrones, cada uno de los átomos al final adopta una estructura de gas noble, quedando ambos rodeados de 8 electrones en sus últimos niveles de energía. Cuando se trata de átomos diferentes, el elemento más electronegativo o no metálico es el que se rodea de ocho electrones.
Observa cómo varió el tamaño
 CLORO GASEOSO
CLORO GASEOSO
SODIO METÁLICO
CLORURO DE SODIO
Observa que al disolverse el ClNa se separan los iones
PROPIEDADES DE LOS COMPUESTOS IÓNICOS
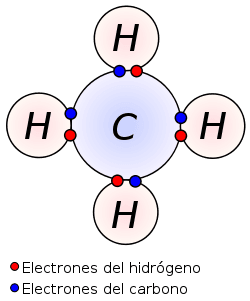

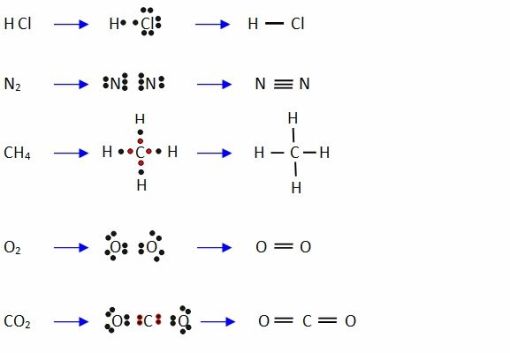
UNIONES COVALENTES
-------------------------------------------------------------------------------------------
UNIONES IÓNICAS
Explicación video
Explicación, propiedades y ejercicios:
Indica el tipo de unión de los sig compuestos
UNIÓN IÓN ICA
|
UNIÓN COVALENTE
|
UNIÓN METÁLICA
|
UNIÓN IÓN ICA
|
UNIÓN COVALENTE
|
UNIÓN METÁLICA
| |||
LiF
|
H2
| |||||||
O3
|
Zn
| |||||||
N2
|
PH3
| |||||||
SO2
|
CO2
| |||||||
NaBr
|
Ca
| |||||||
Cl2
|
S3Fe2
| |||||||
Mg
|
Ni2O3
| |||||||
NH3
|
SH2
|
Grafica según Lewis los compuestos anteriores
Tacha la palabra que no corresponda en el siguiente párrafo
Unión metálica: los átomos (metálicos / no metálicos) tienden a liberar los (protones / electrones) de valencia, transformándose en (iones / átomos sin carga), pero ninguno de ellos los capta, por lo que los electrones permanecen libres moviéndose entre los (cationes / aniones). Los metales son (buenos / malos ) conductores del calor y la electricidad . Son (rígidos / dúctiles)
Unión iónica: Los átomos con mayor tendencia a ( ceder / ganar ) electrones (pierden /ganan) los necesarios para quedar con ( 8 / 18 ) en el último nivel, mientras que los que tienen tendencia a (captar / ceder ) electrones los ganan para completar el octeto. Tienen (alto / bajo) punto de ebullición. En estado sólido, forman cristales (duros / blandos) y quebradizos.
Unión covalente: Los átomos (ceden / comparten ) los electrones y (no / si) forman iones por lo que los compuestos que se obtienen son moleculares. Son (buenos / malos ) conductores del calor y la electricidad. Tienen (bajos / altos ) puntos de fusión y ebullición
Explicación
http://aprenderencasa.educ.ar/aprender-en-casa/alumnos/las_uniones_quimicas.php
http://aprenderencasa.educ.ar/aprender-en-casa/QU%CDMICA%204%B0%20a%F1o%20-%20La%20union%20covalente.pdf
http://aprenderencasa.educ.ar/aprender-en-casa/QU%CDMICA%204%B0%20a%F1o%20-%20Clasificacion%20de%20la%20union%20covalente.pdf
UNIÓN PUENTE HIDRÓGENO
http://www.educ.ar/recursos/ver?rec_id=40711
UNIONES ENTRE MOLÉCULAS
https://www.youtube.com/watch?v=D5dWPyhLlvs














.png)



