Video explicativo formación delpetróleo
https://www.youtube.com/watch?v=gU2UuygQKPI




JUEGO CONSTRUIR MOLÉCULAS
http://www.educaplus.org/game/construye-moleculas-de-alcanos





CICLOALCANOS
Reglas de nomenclatura
http://www.quimicaorganica.org/alcanos/nomenclatura-alcanos/209-nomenclatura-de-alcanos-reglas-iupac.html
Videos explicativos de formulación y nomenclatura
https://www.youtube.com/watch?v=o1-7yBBbD2o
https://www.youtube.com/watch?v=Xt14ghl1GjI
Propiedades físicas
Punto de ebullición: bajo condiciones normales, los alcanos desde el CH4 hasta el C4H10son gases; desde el C5H12 hasta C17H36 son líquidos; y los posteriores a C18H38 son sólidos. El punto de ebullición está determinado principalmente por el peso. Se incrementa entre 20 y 30 °C por cada átomo de carbono agregado a la cadena.
Un alcano de cadena lineal tendrá un mayor punto de ebullición que un alcano de cadena ramificada, debido a la mayor área de la superficie en contacto, con lo que hay mayores fuerzas de van der Waals, entre moléculas adyacentes.
Por otra parte, los cicloalcanos tienden a tener mayores puntos de ebullición que sus contrapartes lineales, debido a las conformaciones fijas de las moléculas, que proporcionan planos para el contacto intermolecular.
Punto de fusión: sigue una tendencia similar al punto de ebullición. A mayor peso molar, mayor punto.
Los alcanos de longitud impar tienen puntos de fusión ligeramente menores, comparados con los alcanos de longitud par. Esto es debido a que los alcanos de longitud par se ordenan bien en la fase sólida, formando una estructura bien organizada, que requiere mayor energía para romperse.
Densidad
La densidad aumenta con el número de átomos de carbono pero siempre es inferior a la del agua, por lo que flotan en la superficie de la misma.
Propiedades Químicas
Tienen una baja reactividad por cuanto sus enlaces son estables, no se rompen con facilidad.
Reaccionan con los halógenos y con el oxígeno en una combustión sin humo.
Usos
Los cuatro primeros alcanos son usados principalmente para propósitos de calefacción y cocina. El metano y el etano son los principales componentes del gas natural
El propano y el butano pueden ser líquidos a presiones moderadamente bajas y son conocidos como gases licuados. Estos dos alcanos son usados también como propelentes en pulverizadores.
Desde el pentano hasta el octano los alcanos son líquidos razonablemente volátiles. Se usan como combustibles en motores de combustión interna. Además de su uso como combustibles, los alcanos medios son buenos solventes para las sustancias no polares.
Los hidrocarburos de 9 a 16 átomos de carbono son líquidos de alta viscosidad y forman parte del diesel y combustible de aviones.
Los alcanos a partir del hexadecano en adelante constituyen los componentes más importantes de los aceites lubricantes.
Los alcanos con una longitud de cadena de aproximadamente 35 o más átomos de carbono se encuentran en el betún y tienen poco valor.
VIDEOS DESTILACIÓN DEL PETRÓLEO
https://www.youtube.com/watch?v=3ejUQfAGYck
https://www.youtube.com/watch?v=UwkqoyZQ-rs
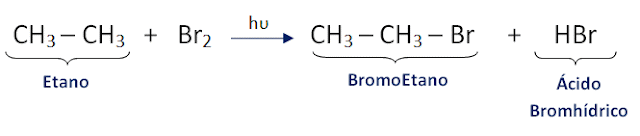
REACCIONES QUÍMICAS
COMBUSTIÓNHALOGENACIÓN